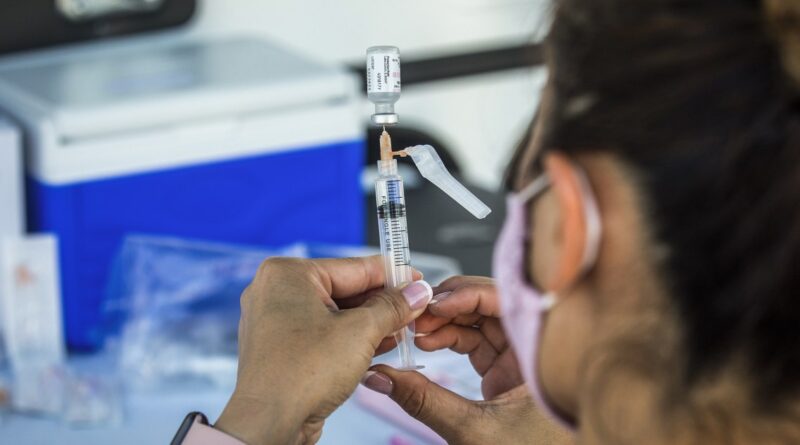
Moderna devrait manquer la date limite du 20 septembre pour l’approbation des boosters
WASHINGTON – Les régulateurs américains ne s’attendent pas à respecter le calendrier du 20 septembre de l’administration Biden consistant à rendre les injections de rappel largement accessibles à ceux qui ont reçu le vaccin Moderna Covid, a déclaré une personne familière avec le processus.
De hauts responsables de la santé ont informé la Maison Blanche qu’ils auront besoin de plus de temps pour examiner la demande de Moderna, car les données que la société a soumises le 1er septembre ont été « jugées inadéquates et doivent être renforcées », a déclaré la personne.
Mais les responsables pensent que les régulateurs sont toujours sur la bonne voie pour prendre une décision sur les rappels du vaccin Pfizer d’ici le 20 septembre. La FDA a prévu une réunion du comité consultatif pour discuter des rappels Pfizer le 17 septembre, a déclaré la personne.
« Ces choses se produisent et font partie du processus », a déclaré la personne. « Nous avons et continuerons de suivre la science. »
De hauts responsables américains de la santé ont annoncé le 18 août que le pays prévoyait de commencer à offrir des injections de rappel de Covid-19 à tous les Américains à partir de la troisième semaine de septembre, citant des preuves que la protection contre l’infection diminuait, alors que la variante delta hautement contagieuse continue de se propager. La date limite non respectée pourrait signifier que seuls ceux qui ont reçu le vaccin de Pfizer peuvent recevoir un rappel pendant au moins plusieurs semaines.
« Nous avons toujours dit que nous suivrions la science et tout cela fait partie d’un processus qui est maintenant en cours », a déclaré le porte-parole de la Maison Blanche, Chris Meagher. « Nous attendons un examen et une approbation complets de la FDA et une recommandation de l’ACIP. Lorsque cette approbation et cette recommandation seront faites, nous serons prêts à mettre en œuvre le plan que les meilleurs médecins de notre pays ont élaboré afin de garder une longueur d’avance sur ce virus. »
Alors que les responsables ont déclaré que le délai dépendait de l’examen de la FDA, il était très inhabituel pour les plus hauts responsables de la santé de faire une recommandation aussi forte avant que la FDA n’ait terminé son travail.
Le New York Times a été le premier à signaler le retard.