Le défi des tests COVID-19

Le défi des tests COVID-19
La pénurie de tests de diagnostic a entravé la réponse américaine à la pandémie de COVID-19, qui a tué plus de 82 000 personnes dans le pays et infecté plus de 1,3 million.
Des tests de diagnostic généralisés pour les cas actifs et des tests d’anticorps pour déterminer qui a déjà été infecté aideront les autorités nationales et locales à décider quand et comment lever les restrictions de séjour à domicile et permettre aux gens de retourner au travail. Mais la plupart des experts s’accordent à dire que la capacité actuelle est loin d’être suffisante.
Le plus grand expert américain des maladies infectieuses, Anthony Fauci, a déclaré que les États-Unis devaient doubler le taux actuel de tests de 1,5 à 2 millions de tests par semaine. Un rapport du Centre d’éthique Edmond J. Safra de l’Université de Harvard indique que les États-Unis doivent être en mesure de tester 5 millions de personnes par jour pour commencer à rouvrir en toute sécurité d’ici juin.
Au 12 mai, les États-Unis avaient effectué environ 9,6 millions de tests de diagnostic pour le nouveau coronavirus depuis le début de l’épidémie.
Tests cumulatifs effectués aux États-Unis
Tests cumulatifs effectués aux États-Unis
Tests cumulatifs effectués aux États-Unis
Essais cumulatifs
exécuté aux États-Unis
Tests cumulatifs effectués aux États-Unis
Source : Le projet de suivi Covid
Les tests de diagnostic sont rares aux États-Unis depuis le début de l’épidémie. Les responsables de la santé se sont initialement appuyés sur des kits de test préparés par les Centers for Disease Control and Prevention, dont certains se sont avérés défectueux. La Food and Drug Administration (FDA) n’a approuvé d’autres tests que le 29 février, plus de cinq semaines après le début des discussions avec des laboratoires extérieurs.
Dans les semaines qui ont suivi, la FDA a autorisé les tests de diagnostic développés par les fabricants et les laboratoires, mais des pénuries intermittentes de fournitures clés ont créé des goulots d’étranglement le long du pipeline de tests.
Matériel nécessaire pour
produire des kits de test
proviennent de sources
autour du monde et
sont très demandés.
Essais et équipement
sont ensuite vendus à des laboratoires
et hôpitaux environ
le pays.
Plusieurs fabricants américains produire
kits et équipements de test.
Matériel nécessaire pour
produire des kits de test
proviennent de sources
autour du monde et
sont très demandés.
Essais et équipement
sont ensuite vendus à des laboratoires
et hôpitaux environ
le pays.
Plusieurs fabricants américains produire
kits et équipements de test.
Matériel nécessaire pour
produire des kits de test
proviennent de sources
autour du monde et
sont très demandés.
Essais et équipement
sont ensuite vendus à des laboratoires
et hôpitaux environ
le pays.
Plusieurs fabricants américains produire
kits et équipements de test.
Plusieurs fabricants américains produire
kits et équipements de test.
Les matériaux nécessaires
produire des tests
les trousses viennent de
sources autour du
monde et sont dans
forte demande.
Essais et équipement
sont ensuite vendus à des laboratoires
et hôpitaux environ
le pays.
Les matériaux nécessaires
produire des tests
les trousses viennent de
sources autour du
monde et sont dans
forte demande.
Essais et
les équipements sont
puis vendu aux labos
et hôpitaux
autour du
pays.
Plusieurs fabricants américains produire
kits et équipements de test.
Les fabricants ont augmenté leur production, mais ils ont été gênés par un manque de composants. New York a été l’État le plus durement touché par le coronavirus, avec plus de 340 000 cas, et le gouverneur Andrew Cuomo a appelé le gouvernement fédéral à superviser l’acquisition et la production de fournitures essentielles afin que les États ne se fassent pas concurrence pour les matériaux.
Cuomo a également annoncé que sept États du nord-est, dont New York, le New Jersey, le Connecticut, le Rhode Island, la Pennsylvanie, le Delaware et le Massachusetts, se sont regroupés pour accroître leur pouvoir de marché et développer une chaîne d’approvisionnement régionale pour les EPI, les tests et les équipements médicaux. Le gouvernement fédéral prévoit d’envoyer suffisamment d’écouvillons et d’équipements connexes dans les 50 États pour couvrir le dépistage d’au moins 2 % de la population.
Il semble que la sécheresse des tests commence à s’améliorer à certains endroits. Los Angeles a annoncé que les tests de diagnostic COVID-19 seront disponibles gratuitement pour tous les résidents, qu’ils présentent des symptômes ou non. Le comté de Los Angeles abrite le plus grand nombre de cas en Californie, avec plus de 33 000. Les lieux de test sont soit sans rendez-vous, soit au volant et nécessitent un rendez-vous, les résultats étant livrés en quelques jours.
Pour comprendre la complexité du processus de test, les étapes des deux tests prédominants – diagnostic et anticorps – sont décrites ci-dessous.
Tests diagnostiques
Un test de réaction en chaîne par polymérase (PCR) est le moyen le plus courant de déterminer si le virus est toujours présent. Ce test fonctionne à la fois pour les personnes symptomatiques et asymptomatiques.
Protection personnelle
l’équipement comprend
des gants, masques, Visage
Boucliers, protecteur
lunettes et robes.
Écouvillons stériles spécialisés
servent à prélever un échantillon
du malade
Stérile spécialisé
écouvillons être habitué
recueillir un échantillon
du malade.
Équipement de protection individuelle
comprend des gants, masques, Visage
Boucliers, lunettes de protection
et robes.
Stérile spécialisé
écouvillons être habitué
recueillir un échantillon
du malade.
Protection personnelle
l’équipement comprend
des gants, masques, Visage
Boucliers, protecteur
lunettes et robes.
Stérile spécialisé
écouvillons être habitué
recueillir un échantillon
du malade
Protection personnelle
l’équipement comprend
des gants, masques, Visage
Boucliers, protecteur
lunettes et robes.
Un écouvillon stérile spécialisé est inséré loin dans la cavité nasale d’un patient pour prélever un échantillon au niveau du nasopharynx, la partie supérieure de la gorge derrière le nez, où le virus est le plus susceptible de se trouver. Les travailleurs de la santé qui collectent des échantillons portent tous un équipement de protection individuelle pour éviter l’infection.
UN solution stérile
conserve le spécimen
pour le transport au laboratoire.
UN solution stérile
conserve le spécimen
pour le transport au laboratoire.
UN solution stérile
conserve le spécimen
pour le transport au laboratoire.
UN solution stérile
préserve la
spécimen pour
transport au laboratoire.
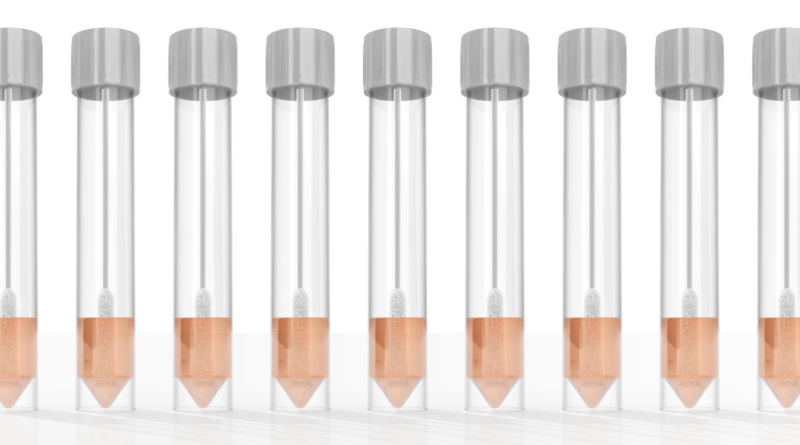
L’écouvillon est placé dans un flacon pour le transport au laboratoire, avec un liquide stérile au fond qui reçoit les cellules collectées. La majorité des tests PCR sont encore effectués en envoyant des échantillons aux laboratoires pour diagnostic. Mais des tests plus récents permettent de collecter et de tester des échantillons sur place, et les résultats peuvent être disponibles en quelques heures.
Les utilisations les plus courantes des tests
produits chimiques spécialisés et
machinerie reproduire n’importe quel
matériel génétique dans un échantillon
et pour tester le virus.
Les utilisations les plus courantes des tests
produits chimiques spécialisés et
machinerie reproduire n’importe quel
matériel génétique dans un échantillon
et pour tester le virus.
Les utilisations les plus courantes des tests
produits chimiques spécialisés et
machinerie reproduire n’importe quel
matériel génétique dans un échantillon
et pour tester le virus.
Les utilisations les plus courantes des tests spécialisé
produits chimiques et machinerie reproduire n’importe quel
matériel génétique dans un échantillon et de tester
le virus.
Une fois dans le laboratoire, les réactifs chimiques sont utilisés en deux étapes – d’abord pour extraire uniquement le matériel génétique du coronavirus du liquide dans le flacon de transport. Ensuite, le matériau isolé est combiné avec d’autres produits chimiques pour reconstruire et répliquer des morceaux du coronavirus à des concentrations suffisamment élevées pour être testées.
Test d’anticorps (sérologique)
Les tests d’anticorps sont différents des tests de diagnostic par prélèvement nasal qui montrent une infection active. Ce sont des tests sanguins destinés à déterminer qui, à un moment donné, a été infecté par le virus et pourrait maintenant être immunisé. Les anticorps, des protéines anti-maladie formées dans les jours et les semaines suivant l’infection, peuvent protéger une personne contre la réinfection, au moins pendant un certain temps, bien qu’il n’ait pas été prouvé que cela soit vrai pour le nouveau coronavirus.
Les deux types d’anticorps sont l’immunoglobuline M (IgM) et l’immunoglobuline G (IgG). Le corps produit rapidement des anticorps IgM pour son attaque initiale contre les infections. Il fabrique les anticorps IgG plus lentement et les retient plus longtemps, suggérant une immunité possible.
Il existe deux formats prédominants pour les tests d’anticorps : l’un utilisant un petit kit moins cher à produire et pouvant renvoyer des résultats en quelques minutes, tandis que l’autre est analysé en laboratoire. Le test de laboratoire est considéré comme plus précis, peut traiter plusieurs échantillons à la fois et montrer combien d’anticorps sont présents.
Le format du kit, illustré ci-dessous, utilise un échantillon de sang prélevé au doigt et renvoie simplement un résultat positif ou négatif pour les deux types d’anticorps produits tout au long de la réponse au virus.
Les patients du sang
échantillon est placé
dans le réservoir.
UN solution tampon est
ajouté à « casser »
structures membranaires
Dans le sang.
Un bande indicatrice sera
signaler la présence de
anticorps à l’intérieur
minutes.
Les patients échantillon de sang
est placé dans le réservoir.
UN solution tampon est ajouté
« casser » la membrane
structures dans le sang.
Un bande indicatrice signalera
la présence d’anticorps
dans quelques minutes.
Les patients échantillon de sang
est placé dans le réservoir.
UN solution tampon est ajouté
« casser » la membrane
structures dans le sang.
Un bande indicatrice signalera
la présence d’anticorps
dans quelques minutes.
Celui d’un patient du sang
échantillon est placé dans
le réservoir.
UN solution tampon est
ajouté à « casser »
structures membranaires
Dans le sang.
Un bande indicatrice sera
signaler la présence de
anticorps en quelques minutes.
Neuf tests d’anticorps avaient été approuvés pour une utilisation d’urgence au 30 avril, y compris ceux réalisés par Ortho Clinical Diagnostics, une société de test établie appartenant à la société de capital-investissement Carlyle Group Inc. Le 4 mai, la FDA a révisé les directives d’autorisation des tests d’anticorps exigeant des fabricants commerciaux , lors de la demande d’autorisation d’utilisation d’urgence de la FDA, pour valider leurs tests d’anticorps et soumettre les données de validation dans un délai de 10 jours.
Sources: Centres pour le Contrôle et la Prévention des catastrophes; Reportage Reuters
Reportage supplémentaire par Allison Martell
Montage par Bill Berkrot et Christine Chan