L’analyse des réclamations administratives dans le monde réel démontre que près de la moitié des patients souffrant de migraines arrêtent l’utilisation de barbituriques après le début de Nurtec ODT
- Les résultats de cette étude démontrent une réduction robuste et cliniquement significative de l’utilisation des barbituriques après le début de Nurtec ODT, offrant une thérapie alternative contre la migraine pour ceux qui peuvent dépendre du butalbital ou qui souhaitent une thérapie alternative qui n’est pas associée à un potentiel de dépendance.
- Bien qu’ils soient associés à un potentiel de dépendance, à des maux de tête de surconsommation de médicaments (rebonds) et à des effets secondaires sur le système nerveux central, les barbituriques sont prescrits comme traitements de première intention contre la migraine.
- Les réclamations médicales et de prescription longitudinales ont été utilisées pour évaluer les prescriptions de barbituriques et les milligrammes moyens dispensés chez les patients migraineux observés 6 mois avant et après l’initiation de Nurtec ODT.
- Parmi les 24 359 migraineux qui utilisaient du butalbital avant de commencer le traitement avec Nurtec ODT, environ 49 % n’avaient pas de prescription de butalbital dans les 6 mois suivant le début.
NEW HAVEN, Conn., 31 août 2022 /PRNewswire/ — Biohaven Pharmaceutical Holding Company Ltd. (NYSE : BHVN) a annoncé les conclusions importantes concernant les avantages de Nurtec® ODT (rimegepant) pour réduire le fardeau de l’utilisation du butalbital chez les patients migraineux dans la pratique clinique du monde réel.
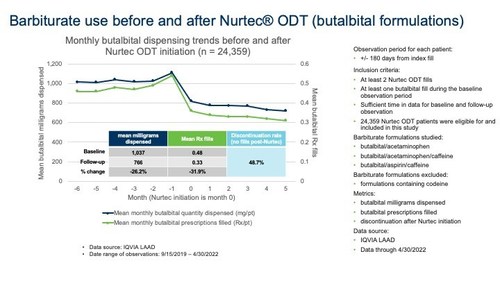
Figure 1
Noé RosenMD, Northwell Physician Partners, Neuroscience Institute of Grand cou, NY a commenté: « Les prescriptions de composés contenant du butalbital restent élevées malgré les questions de longue date sur la sécurité dans d’autres conditions, les effets secondaires potentiels importants, les interactions médicamenteuses multiples et le risque de dépendance et de mauvaise utilisation. » Neurologue, Katherine Standley DO., directeur médical de Biohaven, a déclaré : « Le butalbital présente un risque élevé d’entraîner des maux de tête par abus de médicaments, et a conduit l’American Academy of Neurology (AAN) et l’American Headache Society (AHS) à recommander d’éviter son utilisation en première intention. agent dans le traitement des maux de tête. »
La population à l’étude a été dérivée d’une base de données longitudinale et anonymisée intégrée sur les demandes de remboursement de frais médicaux et d’ordonnances de 15 septembre 2019 à travers 30 avril, 2022. Les données contiennent des réclamations au niveau du patient avec des informations sur le plan, le payeur, l’établissement, la procédure, les médicaments et le diagnostic. La période d’observation pour chaque patient était de +/- 180 jours à partir du remplissage de l’index. Pour être inclus dans l’étude, le patient devait avoir rempli au moins 2 ordonnances Nurtec ODT, avoir au moins un remplissage de butalbital pendant la période d’observation de base et avoir suffisamment de temps dans les données pour l’observation de base et de suivi. Les formulations de barbituriques étudiées comprenaient le butalbital/acétaminophène, le butalbital/acétaminophène/caféine et le butalbital/aspirine/caféine. Les formulations de barbituriques contenant de la codéine ont été exclues.
Parmi les 491 149 patients Nurtec, 24 359 répondaient aux critères d’inclusion et sont décrits dans la figure 1 ci-dessous. Le taux global d’abandon du butalbital après le début du Nurtec ODT était de 48,7 %. Dans l’ensemble, le nombre moyen d’ordonnances mensuelles de butalbital a diminué de 31,9 % et le nombre moyen de milligrammes distribués a diminué de 26,2 %.
Gil L’Italien Ph.D., vice-président principal, GHEOR et épidémiologie, Biohaven, a commenté : « Malgré les directives de traitement suggérant que les barbituriques doivent être évités pour le traitement de la migraine en première ligne en raison du potentiel de dépendance, des effets sur le système nerveux central et des médicaments céphalées de surmenage, les barbituriques sont prescrits en pratique clinique, parfois en première intention chez les patients qui ne sont pas candidats aux triptans. l’opportunité d’évaluer les tendances associées à ces transitions. Nos résultats confirment les avantages de Nurtec ODT en tant que traitement efficace et sûr de la migraine qui peut réduire le besoin de barbituriques.
Le Dr Rosen a en outre commenté : « Cette étude a donné un aperçu du monde réel de l’impact que l’offre d’un traitement plus spécifique peut avoir sur l’éloignement de l’utilisation de médicaments par rapport aux anciens remèdes non spécifiques. De plus, en lançant Nurtec ODT, non seulement les patients ont réduit le butalbital l’utilisation concomitante de caféine, d’acétaminophène ou d’aspirine en raison de leur présence dans ces analgésiques combinés. »
Le Dr Standley a ajouté : « Avant l’institution des antagonistes du CGRP, comme Nurtec ODT, nous avions des options limitées pour la prise en charge aiguë de la migraine chez les patients intolérants ou non candidats aux traitements par les triptans. Les médicaments tels que les opioïdes et les barbituriques contenant des analgésiques sont associés à potentiel de dépendance et risque accru de migraine chronique. Ces données confirment que l’initiation de Nurtec ODT est associée à une réduction significative de l’utilisation du butalbital dans les données du monde réel. Lorsqu’elles sont associées aux données sur les opioïdes présentées précédemment, cela suggère une réduction globale de l’utilisation de médicaments contrôlés. substances avec l’initiation de Nurtec ODT. »
NURTEC ODT (rimegepant) a été approuvé par la Food and Drug Administration (FDA) des États-Unis pour le traitement aigu de la migraine chez les Février 2020 et pour le traitement préventif de la migraine épisodique chez Mai 2021.
À propos de NURTEC ODT
NURTEC ODT (rimegepant) est le premier et le seul antagoniste des récepteurs du peptide lié au gène de la calcitonine (CGRP) disponible dans une formulation ODT à dissolution rapide approuvée par la Food and Drug Administration (FDA) des États-Unis pour le traitement aigu de la migraine avec ou sans aura et le traitement préventif de la migraine épisodique chez l’adulte. On pense que l’activité du neuropeptide CGRP joue un rôle causal dans la physiopathologie de la migraine. NURTEC ODT est un antagoniste des récepteurs CGRP qui agit en bloquant de manière réversible les récepteurs CGRP, inhibant ainsi l’activité biologique du neuropeptide CGRP. La dose recommandée de NURTEC ODT est de 75 mg, à prendre au besoin, jusqu’à une fois par jour pour traiter ou tous les deux jours pour aider à prévenir les crises de migraine. Pour plus d’informations sur NURTEC ODT, visitez www.nurtec.com.
Indication
Les comprimés à désintégration orale NURTEC ODT sont un médicament sur ordonnance utilisé pour traiter la migraine chez les adultes. Il est destiné au traitement aigu des crises de migraine avec ou sans aura et au traitement préventif de la migraine épisodique. On ne sait pas si NURTEC ODT est sûr et efficace chez les enfants.
Informations importantes sur la sécurité
Ne prenez pas NURTEC ODT si vous êtes allergique à NURTEC ODT (rimegepant) ou à l’un de ses ingrédients.
Avant de prendre NURTEC ODT, informez votre fournisseur de soins de santé (HCP) de toutes vos conditions médicales, y compris si vous :
- avez des problèmes de foie,
- avez des problèmes rénaux,
- êtes enceinte ou envisagez de devenir enceinte,
- allaitez ou envisagez d’allaiter.
Informez votre professionnel de la santé de tous les médicaments que vous prenez, y compris les médicaments sur ordonnance et en vente libre, les vitamines et les suppléments à base de plantes.
NURTEC ODT peut provoquer des effets secondaires graves, notamment des réactions allergiques, des difficultés respiratoires et des éruptions cutanées. Cela peut se produire plusieurs jours après la prise de NURTEC ODT. Appelez votre professionnel de la santé ou obtenez immédiatement une aide d’urgence si vous avez un gonflement du visage, de la bouche, de la langue ou de la gorge ou des difficultés respiratoires. Cela s’est produit chez moins de 1 % des patients traités par NURTEC ODT.
Les effets secondaires les plus fréquents de NURTEC ODT étaient les nausées (2,7 %) et les douleurs à l’estomac/indigestion (2,4 %). Ce ne sont pas les seuls effets secondaires possibles de NURTEC ODT. Dites à votre HCP si vous avez des effets secondaires.
Nous vous encourageons à signaler les effets secondaires des médicaments sur ordonnance à la FDA.
Visitez www.fda.gov/medwatch ou appelez le 1-800-FDA-1088 ou signalez les effets secondaires à Biohaven au 1-833-4NURTEC.
Voir les renseignements posologiques complets et les renseignements pour les patients.
À propos de la migraine
Près de 40 millions de personnes aux États-Unis souffrent de migraine et l’Organisation mondiale de la santé classe la migraine parmi les 10 maladies médicales les plus invalidantes. La migraine est caractérisée par des crises débilitantes d’une durée de quatre à 72 heures avec de multiples symptômes, y compris des maux de tête pulsés d’intensité de douleur modérée à sévère qui peuvent être associés à des nausées ou des vomissements, et/ou une sensibilité au son (phonophobie) et une sensibilité à la lumière (photophobie). Il existe un important besoin non satisfait de nouveaux traitements, car plus de 90 % des personnes souffrant de migraine sont incapables de travailler ou de fonctionner normalement pendant une crise.
Antagonisme des récepteurs CGRP
Les antagonistes des récepteurs CGRP à petites molécules représentent une nouvelle classe de médicaments pour le traitement de la migraine. Les antagonistes des récepteurs CGRP agissent en bloquant de manière réversible les récepteurs CGRP, inhibant ainsi l’activité biologique du neuropeptide CGRP. Pour le traitement aigu, ce mode d’action unique offre potentiellement une alternative aux autres agents, en particulier pour les patients qui ont des contre-indications à l’utilisation des triptans ou qui ont une mauvaise réponse ou une intolérance aux triptans. Les thérapies bloquant le signal CGRP n’ont pas été associées à des céphalées par surutilisation de médicaments (MOH) ou à des céphalées de rebond, ce qui limite l’utilité clinique d’autres traitements aigus en raison de l’augmentation des crises de migraine résultant d’une utilisation fréquente.
À propos de Biohaven
Biohaven est une société biopharmaceutique mondiale au stade commercial avec un portefeuille de thérapies innovantes et de premier ordre pour améliorer la vie des patients atteints de maladies neurologiques et neuropsychiatriques débilitantes, y compris des troubles rares. Le portefeuille Neuroinnovation™ de Biohaven comprend Nurtec ODT (rimegepant) approuvé par la FDA pour le traitement aigu et préventif de la migraine Approuvé par l’EMA sous le nom de Vydura® pour le traitement aigu de la migraine avec ou sans aura, et la prophylaxie de la migraine épisodique chez les adultes qui crises de migraine par mois) et un large portefeuille de produits candidats de stade avancé sur cinq plateformes mécanistes distinctes : antagonisme des récepteurs CGRP pour le traitement aigu et préventif de la migraine ; modulation du glutamate pour le trouble obsessionnel-compulsif et l’ataxie spinocérébelleuse ; et l’inhibition de la MPO pour la sclérose latérale amyotrophique ; Kv7 Ion Channel Activators (Kv7) activateurs de l’épilepsie focale et de l’hyperexcitabilité neuronale, et inhibition de la myostatine pour les maladies neuromusculaires. Plus d’informations sur Biohaven sont disponibles sur www.biohavenpharma.com.
Énoncés prospectifs
Ce communiqué de presse contient des déclarations prospectives au sens de la loi Private Securities Litigation Reform Act de 1995. Ces déclarations prospectives impliquent des risques et des incertitudes substantiels, y compris des déclarations basées sur les attentes et hypothèses actuelles de la direction de Biohaven concernant NURTEC ODT comme un traitement aigu pour les patients souffrant de migraine et un traitement préventif de la migraine. Les facteurs susceptibles d’affecter ces déclarations prospectives comprennent ceux liés à : la capacité de Biohaven à commercialiser efficacement NURTEC ODT, des retards ou des problèmes dans l’approvisionnement ou la fabrication de NURTEC ODT, la conformité aux exigences réglementaires américaines applicables, le calendrier, le début et les résultats attendus de Biohaven les essais cliniques prévus et en cours ; le calendrier des interactions prévues et des dépôts auprès de la FDA ; le calendrier et le résultat des dépôts réglementaires attendus ; la commercialisation potentielle des produits candidats de Biohaven ; le potentiel pour les produits candidats de Biohaven d’être les premiers ou les meilleurs traitements de leur catégorie ; et l’efficacité et la sécurité des produits candidats de Biohaven. Divers facteurs importants pourraient faire en sorte que les résultats ou événements réels diffèrent sensiblement de ceux qui peuvent être exprimés ou sous-entendus dans les déclarations prospectives. D’autres facteurs importants à prendre en compte dans le cadre des déclarations prospectives sont décrits dans la section « Facteurs de risque » du rapport annuel de Biohaven sur formulaire 10-K déposé auprès de la Securities and Exchange Commission le 25 février 2022, et dans les documents déposés ultérieurement par Biohaven auprès de la Securities and Exchange Commission. Les déclarations prospectives sont faites à la date de ce communiqué, et Biohaven n’assume aucune obligation de mettre à jour les déclarations prospectives, que ce soit à la suite de nouvelles informations, d’événements futurs ou autrement, sauf si la loi l’exige.
NURTEC et NURTEC ODT sont des marques déposées de Biohaven Pharmaceutical Ireland DAC. Neuroinnovation est une marque déposée de Biohaven Pharmaceutical Holding Company Ltd.
Contact
Jennifer Porcelli
Vice-président, Relations avec les investisseurs
[email protected]
201-248-0741
Personne-ressource pour les médias
Mike Beyer
Sam Brown Inc.
[email protected]
312-961-2502
SOURCE Biohaven Pharmaceutical Holding Company Ltd.


