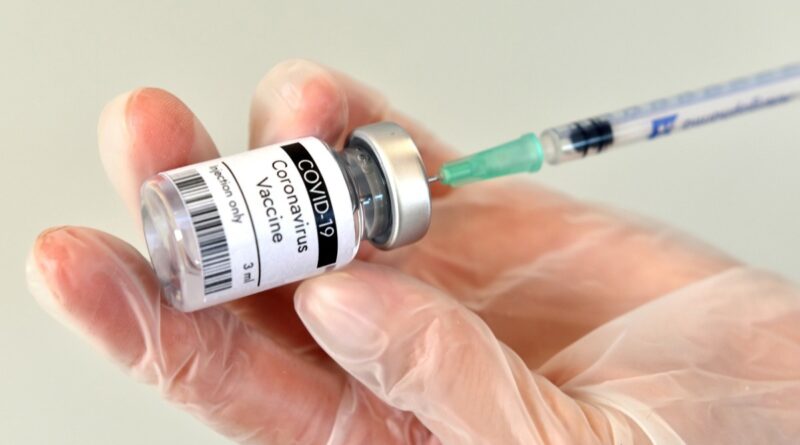
Le vaccin SARS-CoV-2 de Pfizer n’affecte pas la phase de lune de miel du diabète de type 1
Dans une étude récente publiée dans Vaccinsles chercheurs ont rapporté que le vaccin BNT162b2 de Pfizer contre le coronavirus 2 du syndrome respiratoire aigu sévère (SRAS-CoV-2) n’affecte pas la phase de lune de miel du diabète de type 1 (DT1).
Le diabète a été considéré comme un facteur de risque de morbidité et de mortalité par maladie à coronavirus 2019 (COVID-19). Bien que les vaccins COVID-19 existants aient considérablement réduit la morbidité et la mortalité, de nombreux rapports d’hyperglycémie induite par la vaccination (ViHG) et d’autres complications associées ont fait surface.
Diverses études ont rapporté que certains patients atteints de DT1 éprouvent une instabilité transitoire de la glycémie après la vaccination contre la COVID-19, qui se résorbe en quelques jours. Cependant, l’impact de la vaccination contre le SRAS-CoV-2 sur la phase de rémission clinique du DT1, connue sous le nom de phase de lune de miel, reste incertain.
L’étude et les conclusions
Dans la présente étude, les chercheurs ont décrit le cas d’un patient DT1 qui a reçu le vaccin BNT162b2 pendant la phase de lune de miel. Le sujet était un Italien de 24 ans diagnostiqué DT1 en juillet 2020 après une hyperglycémie sévère avec acidocétose diabétique modérée (ACD) nécessitant une hospitalisation.
Le patient a été initialement traité avec de l’insuline intraveineuse et de l’insuline sous-cutanée après la résolution de l’ACD. Un nutritionniste a prescrit un régime méditerranéen (1,8 kilo calories/jour). Le patient est sorti après cinq jours d’admission. La dose quotidienne totale d’insuline a été réduite progressivement lors des visites de suivi ambulatoires en raison de jeûnes fréquents et d’épisodes hypoglycémiques postprandiaux.
L’insuline basale à faible dose a été maintenue après 30 jours. Le sujet a subi un test de tolérance aux repas mixtes (MMTT) deux mois après le début de l’ACD et la résolution de l’hyperglycémie. La valeur du peptide de connexion à jeun (peptide C) était de 0,74 ng/ml et la valeur maximale était de 2,95 ng/ml. Le patient est déjà passé à la phase de lune de miel, indiquée par une hémoglobine A1c ajustée à la dose d’insuline (IDAA1c) [a marker for clinical remission of T1D] valeur de 5,66.
Les tests de laboratoire tels que la numération globulaire complète, le profil lipidique, les marqueurs des fonctions hépatique, thyroïdienne et rénale, et ceux de la maladie cœliaque et de l’auto-immunité thyroïdienne étaient sans particularité. Quatorze mois après le diagnostic de DT1, lors d’un MMTT de suivi, le sujet a montré une fonction résiduelle des cellules bêta préservée.
Le cas était encore sur une faible dose d’insuline. Le sujet a reçu le premier vaccin BNT162b2 le 13 décembre 2021 et le second le 3 janvier 2022. Après la première dose, le patient a connu une détérioration du contrôle glycémique ; c’est-à-dire que la fréquence des épisodes hyperglycémiques postprandiaux a augmenté modérément, et cette tendance s’est particulièrement aggravée après la deuxième vaccination. Cela a incité la reprise des injections d’insuline au moment des repas pendant une semaine.
Le profil glycémique ambulatoire a été obtenu à partir d’un capteur de glucose sous-cutané 1) 21 jours avant la première vaccination, 2) 21 jours après la première dose, 3) 21 jours après la deuxième dose et 4) 42 jours après la deuxième vaccination. Les auteurs ont noté que la détérioration du contrôle glycémique résultait de la vaccination, particulièrement plus évidente après l’administration de la deuxième dose.
Aucun épisode significatif d’hypoglycémie n’a été observé lors des visites de suivi, et aucun événement indésirable n’est survenu après la première ou la deuxième vaccination. Lors d’un MMTT trois mois après la deuxième vaccination, soit 19 mois après le début du DT1, les auteurs ont observé de manière inattendue que le patient était encore en phase de lune de miel. Cela a été confirmé par une valeur IDAA1c de 6,1. Il n’y a pas eu de changements substantiels dans la sécrétion endogène résiduelle d’insuline ou dans les besoins quotidiens en insuline.
Un dosage immunologique des microparticules chimiluminescentes a été réalisé trois mois après l’administration de la seconde dose. Il a révélé la présence de titres élevés d’anticorps anti-SARS-CoV-2 neutralisant l’immunoglobuline G (IgG) et l’absence d’anticorps neutralisants IgM, indiquant que la réponse humorale des anticorps contre le SARS-CoV-2 était robuste après un schéma à deux doses.
conclusion
Les auteurs ont rapporté que la vaccination avec deux doses du vaccin BNT162b2 n’a pas d’impact négatif sur la phase de lune de miel ou sur la fonction des cellules bêta résiduelles. La vaccination n’a provoqué qu’un ViHG temporaire sans influencer de manière significative le déroulement de la phase de lune de miel. Le vaccin n’a pas déclenché ou exacerbé l’auto-immunité des îlots. Ces résultats peuvent encourager la vaccination contre le SRAS-CoV-2 chez les patients atteints de DT1 pendant leur phase de lune de miel et aider à surmonter le scepticisme vis-à-vis du vaccin observé chez bon nombre de ces patients.
Néanmoins, il est essentiel de délimiter dans de grandes études prospectives l’impact immunométabolique et la sécurité du vaccin chez les patients DT1 pendant la phase de lune de miel. Les chercheurs ont suggéré que les patients atteints de DT1 soient convenablement conseillés sur la possibilité de ViHG transitoire et strictement surveillés après la vaccination lors des visites ambulatoires.
Référence de la revue :
- Infante, M.; Fabbri, A.; Padilla, N.; Pacifici, F.; Di Perna, P.; Vitiello, L.; Feraco, A.; Giuliano, M.; Passeri, M.; Caprio, M.; et coll. (2022). Le vaccin BNT162b2 ARNm COVID-19 n’a pas d’impact sur la phase de lune de miel dans le diabète de type 1 : un rapport de cas. Vaccins. est ce que je: https://doi.org/10.3390/vaccines10071096 https://www.mdpi.com/2076-393X/10/7/1096