La campagne de rappel de COVID-19 aux États-Unis ne commencera qu’avec Pfizer – source
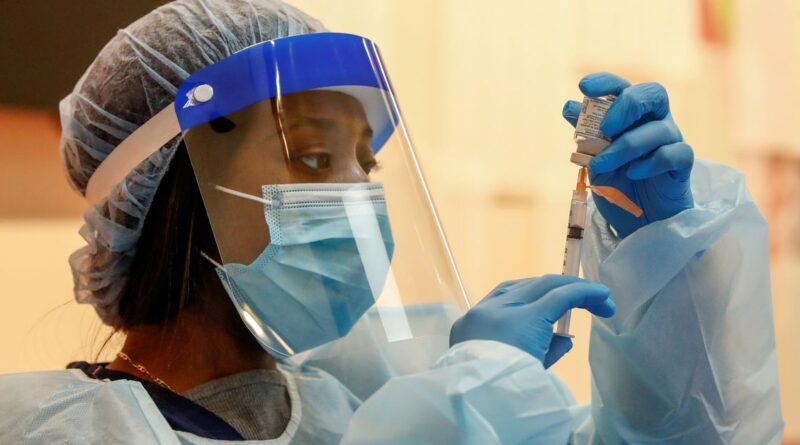
L’assistante médicale Mariasha Davis aspire le vaccin Moderna COVID-19 dans une seringue avant que les gens ne soient inoculés à la Trinity United Church of Christ à Chicago, Illinois, États-Unis, le 13 février 2021. REUTERS/Kamil Krzaczynski/File Photo
WASHINGTON, 3 septembre (Reuters) – Un plan de la Maison Blanche visant à offrir des injections de rappel COVID-19 ne commencera probablement ce mois-ci qu’avec le vaccin fabriqué par Pfizer Inc (PFE.N) et BioNTech (22UAy.DE), une initiative plus étroite que prévu, a déclaré vendredi une source proche du dossier.
Le président Joe Biden avait prévu de lancer une campagne pour administrer 100 millions de rappels le 20 septembre. Mais les fabricants de vaccins américains autres que Pfizer ont tardé à demander l’autorisation d’une dose supplémentaire.
Moderna Inc (MRNA.O) n’a commencé à soumettre des données pour l’approbation réglementaire d’un rappel que mercredi et a déclaré vendredi avoir terminé sa soumission.
Un panel d’experts qui conseille la FDA sur les vaccins prévoit de se réunir le 17 septembre pour discuter des doses supplémentaires du vaccin Pfizer. Il n’est pas clair si la Food and Drug Administration aura suffisamment de temps pour examiner la soumission de Moderna avant la réunion.
Johnson & Johnson (JNJ.N) n’a pas encore demandé aux régulateurs d’approuver un rappel pour son injection à dose unique, et a déclaré la semaine dernière qu’il était en discussion avec la FDA à ce sujet.
Plus tôt, le New York Times a rapporté que les responsables avaient demandé jeudi à la Maison Blanche de réduire un plan visant à offrir les injections de rappel au grand public plus tard ce mois-ci.
Alors que les infections de la variante Delta augmentent, l’administration Biden craint que les infections à COVID chez les personnes entièrement vaccinées soient un signe que la protection vaccinale diminue. Il a poussé les boosters comme moyen de reconstruire l’immunité.
« Nous attendons un examen complet et l’approbation de la FDA » et des conseillers des Centers for Disease Control and Prevention (CDC), a déclaré le porte-parole de la Maison Blanche, Chris Meagher.
« Lorsque cette approbation et cette recommandation seront faites, nous serons prêts à mettre en œuvre le plan élaboré par les meilleurs médecins de notre pays afin que nous gardions une longueur d’avance sur ce virus. »
Le Dr Janet Woodcock, commissaire par intérim de la FDA, et le Dr Rochelle Walensky, directrice du CDC, ont déclaré jeudi au coordinateur COVID de la Maison Blanche Jeffrey Zientz que leurs agences pourraient être en mesure de recommander des rappels d’ici fin septembre uniquement pour certains receveurs du vaccin Pfizer-BioNTech, la source familier avec les discussions dit.
Les autorités sanitaires américaines avaient déclaré en août qu’une troisième injection serait largement accessible le 20 septembre aux Américains ayant reçu deux doses des vaccins Pfizer-BioNTech ou Moderna au moins huit mois plus tôt.
Le plan de rappel américain dépend de la détermination par la Food and Drug Administration qu’une troisième dose des vaccins à deux doses est sûre et efficace et d’une recommandation favorable des conseillers du CDC.
Les porte-parole de la FDA et du CDC ont renvoyé des questions à la Maison Blanche.
Reportage d’Ahmed Aboulenein; Reportages supplémentaires de Michael Erman dans le New Jersey, Julie Steenhuysen à Chicago et Doina Chiacu et Jeff Mason à Washington; édité par Steve Orlofsky, Caroline Humer, David Gregorio et Cynthia Osterman
Nos normes : les principes de confiance de Thomson Reuters.