Données du monde réel: comment tirer parti des sources de données transformatrices pour réduire les coûts des études, évaluer les résultats cliniques du monde réel
Faits et chiffres. Commençons par certains pour expliquer pourquoi les données du monde réel (RWD) et les preuves du monde réel (RWE) qu’elles fournissent continuent de gagner en importance. RWD et RWE apportent une valeur croissante aux entreprises de technologie pharmaceutique et médicale (MedTech) pour accélérer les délais d’étude, raccourcir les délais de mise sur le marché, démontrer l’innocuité et l’efficacité, et même maximiser le succès commercial.
- Dans un rapport publié basé sur une enquête sectorielle de 2020, plus de 80% des entreprises répondantes ont indiqué qu’elles concluent des partenariats stratégiques pour accéder à de nouvelles sources de RWD.1
- Presque toutes les entreprises prévoient d’augmenter leurs investissements dans les talents, la technologie et les partenariats externes pour renforcer leurs capacités RWE.2
- 90% des personnes interrogées ont déclaré avoir déjà établi ou investir actuellement dans la création de capacités RWE à utiliser tout au long du cycle de vie du produit, mais seulement 45% ont des capacités suffisamment matures pour le faire.3
- La FDA a publié une analyse de 90 exemples utilisant RWE pour soutenir la prise de décision réglementaire dans MedTech.4
Bien que RWD et RWE ne soient en aucun cas nouveaux, ce qui est nouveau, c’est l’accent accru mis sur leur prévalence et la valeur que ces données et preuves continueront de fournir aux entreprises pharmaceutiques et MedTech tout au long du cycle de vie d’un produit.
Le moment est venu d’adopter RWD et RWE.
RWD constitue la base de RWE et peut être extrait d’un large éventail de sources, mais tous les RWD ne sont pas créés de la même manière.
La mesure dans laquelle les données peuvent fournir des preuves précieuses dépend de l’utilisation appropriée de la ou des sources de données les plus pertinentes, ainsi que de la dépendance à l’utilisation appropriée de l’expertise dans l’analyse et la communication des résultats des études. Une recherche de haute qualité peut être obtenue grâce à une collaboration précoce avec le bon partenaire, de la conception à la livraison.

Se préparer: comment sélectionner des données du monde réel
La pertinence et la fiabilité des données sont essentielles pour garantir que RWD et les preuves générées peuvent être utilisées de manière appropriée pour soutenir la prise de décision.
Avant de plonger la tête la première, les chercheurs doivent définir une question de recherche clinique claire et travailler avec leurs parties prenantes concernées pour développer un plan d’étude le plus susceptible d’aboutir à des réponses cliniquement robustes. Il n’existe pas d’approche universelle pour sélectionner le RWD.
Certains facteurs à prendre en compte lors de la sélection de RWD comprennent5:
- Les éléments de données à collecter
- Définitions des éléments de données
- Méthodes d’agrégation des données
- Délais pertinents pour la collecte des éléments de données
Bien que ces facteurs puissent guider les critères de sélection des sources RWD, le ou les ensembles de données de mots réels doivent être évalués pour déterminer s’ils sont aptes à l’emploi. Voici trois considérations clés pour y parvenir:
- Disponibilité: Quelles données sont disponibles? Les informations peuvent-elles être obtenues de manière éthique et efficace?
- Pertinence: Dans quelle mesure les sources de données sont-elles pertinentes? Les données sont-elles capables de répondre aux questions de recherche souhaitées?
- Fiabilité: Quelle est la fiabilité des données? Quelle est la probabilité que l’ensemble de données fournisse une réponse suffisamment solide?6
Comment se procurer des données du monde réel pour développer des preuves du monde réel de haute qualité
La prochaine étape consiste à trouver les bonnes données du monde réel pour vos besoins uniques. À quoi ressemble ce processus? Quelles sont certaines des sources courantes de RWD dans les soins de santé?
Bien qu’il existe un large éventail de sources RWD, chacune a ses forces et ses limites. Mais lorsque vous prenez en compte la possibilité de lier plusieurs sources de données américaines, la valeur fournie par RWD augmente de façon exponentielle.
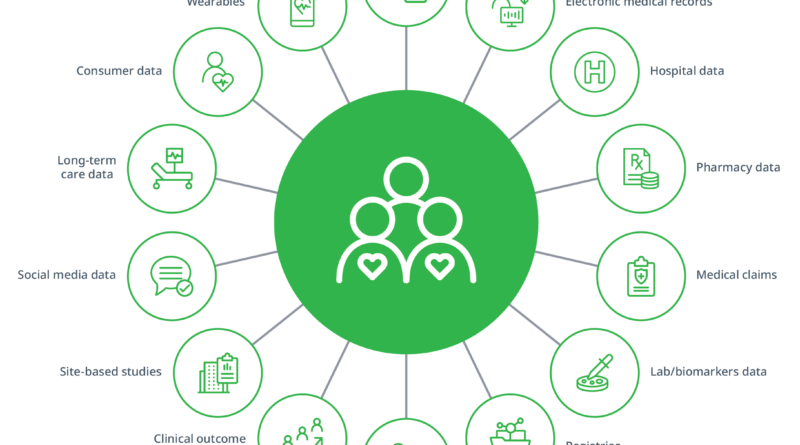
Voici un aperçu de six des sources RWD d’IQVIA qui peuvent être exploitées et reliées entre elles, ainsi que reliées à d’autres sources de données externes (par exemple, les registres de patients, les données fournies par les clients) pour obtenir des résultats avec succès.7
- Base de données des demandes de règlement de santé: PharMetrics® Plus d’IQVIA fournit une base de données longitudinale des réclamations médicales et pharmaceutiques jugées, avec des données remontant à 2006.
- Dossiers médicaux électroniques (DME): Cela comprend le DME ambulatoire d’IQVIA (AEMR) ainsi que les DME spécialisés tels que son DME en oncologie.
- Maître des données de charge (CDM): Cette source de données comprend plus d’une décennie de données provenant d’hôpitaux généraux non fédéraux à court terme. Il suit les patients de tous les types de paie, fournit un plus grand niveau de détails sur ce qui se passe pendant les visites à l’hôpital et va au-delà des données standard sur les demandes de règlement des hôpitaux.
- Allégations longitudinales sur ordonnance (LRx): Cette source de données comprend des actifs de données longitudinales sur les ordonnances des patients comprenant des données sur les pharmacies de détail, de courrier et de soins de longue durée.
- Réclamations médicales (Dx): Présentant 1,1 milliard de réclamations annuelles, les données Dx d’IQVIA sont collectées à partir de services fournis dans les cabinets de médecins à travers les États-Unis.Les données comprennent le diagnostic au niveau des patients, les procédures et les traitements en cabinet pour les visites effectuées principalement auprès de professionnels en cabinet aux États-Unis dans tous les cabinets médicaux, hôpitaux, centres de chirurgie ambulatoire et autres pratiques de soins de santé.
- Offres de données de laboratoire: Les données de laboratoire fournissent des résultats de données approfondies de laboratoire, de génomique et de biomarqueurs. IQVIA recueille ces données via un vaste réseau de chaînes nationales de laboratoires indépendants, d’agrégateurs de données de laboratoire et de laboratoires spécialisés. Des milliers de résultats de laboratoire différents sont disponibles dans cette offre de données pour différents segments de marché.
Équipé du vaste éventail de sources de données répertoriées, combiné à la possibilité de les lier, quelle est la prochaine étape? Comment RWD peut-il être mis à profit dans une étude du monde réel? L’étude de cas suivante en fournit une démonstration.
Étude de cas: Tirer parti des données du monde réel pour mesurer le coût associé à la gravité chez les patients atteints de sclérose en plaques (SEP)8
Il existe de nombreuses mesures d’une maladie qui sont des indicateurs importants pour les patients, les payeurs et les prestataires, mais qui sont difficiles à mesurer en utilisant uniquement les données des réclamations. Pensez à la sclérose en plaques (SEP). La gravité de cette maladie, telle que définie par le niveau d’incapacité, a un impact direct sur la gestion de la maladie et les résultats pour les patients. Le niveau de progression de l’invalidité de la SEP est le plus souvent mesuré à l’aide de l’échelle élargie de l’état d’incapacité de Kurtzke (EDSS).

Les scores EDSS ne sont généralement pas disponibles dans les sources RWD facilement disponibles, y compris les bases de données de DME et de réclamations administratives de soins de santé. Cependant, les chercheurs d’IQVIA ont récemment démontré qu’il est possible de définir le niveau d’incapacité chez les patients atteints de SEP en utilisant les éléments individuels de l’EDSS pour traduire et analyser les données du DME, puis en corroborant ces résultats grâce à une analyse des données des demandes de règlement de santé.
Le processus
Tout d’abord, tous les patients atteints de SEP dans la base de données AEMR d’IQVIA ont été identifiés. La base de données contient des données de 76 millions de patients à travers les États-Unis datant de 2006 et est l’une des plus grandes bases de données de DME couplables de l’industrie. Des éléments de l’EDSS ont été identifiés dans les tableaux de diagnostic et de liste des problèmes.
En collaboration avec un panel d’experts en SP, les chercheurs d’IQVIA ont attribué un niveau de gravité à chaque symptôme lié à l’EDSS et ont utilisé une affectation pour mapper les enregistrements aux codes de facturation, en joignant une mesure de l’invalidité à chaque patient. L’algorithme a été spécialement conçu pour suivre l’évolution des niveaux de gravité des symptômes au fil du temps, et pour noter quand les patients présentaient plus d’un symptôme ou état – un léger mais un autre (d’autres) sévère. Par exemple, dans le système pyramidal responsable du mouvement moteur, la faiblesse périphérique pourrait être considérée comme un léger symptôme de handicap, alors que la paraplégie serait associée à une forme de handicap beaucoup plus sévère.
Ensuite, tous les patients atteints de SEP dans le DME ont été liés à la base de données des réclamations PharMetrics® Plus d’IQVIA. Au total, 45 687 patients ont été identifiés dans la base de données du DME et 1 599 ont été liés à la base de données des réclamations.
À l’aide de l’algorithme du handicap, les symptômes ont été suivis pour évaluer leur évolution chez les patients légers, modérés et sévères, et pour quantifier les implications financières connexes de ces tendances.
Les résultats
L’étude a révélé que les coûts ajustés des soins de santé étaient 15% plus élevés chez les patients avec une incapacité modérée que chez les patients avec une incapacité légère, et 20% plus élevés chez les patients avec une incapacité sévère par rapport à ceux avec une incapacité légère. Il montre également que les coûts des thérapies modificatrices de la maladie (DMT) représentaient respectivement 89%, 82% et 78% des coûts de pharmacie ambulatoire chez les patients présentant une incapacité légère, modérée et sévère.
Cette étude, récemment publiée dans le Journal of Medical Economics, est le premier du genre à montrer comment un algorithme basé sur les réclamations peut être utilisé pour estimer l’invalidité de la SP en utilisant les données des DME.
Cela prouve que des données complexes sur les maladies peuvent être tirées de ces ressources RWD, offrant ainsi l’opportunité d’examiner les résultats en l’absence de marqueurs standard de la progression de la maladie.
Conclusion: RWD continuera à ajouter de la valeur
Il ne fait aucun doute que RWD ajoute une valeur considérable au processus de recherche. Cependant, trouver la bonne combinaison de données inégalées, la bonne méthodologie pour votre étude et le bon partenaire peut être compliqué.
Dans le marché des sciences de la vie hautement concurrentiel d’aujourd’hui, les données connectées doivent faire partie de l’écosystème des preuves pour soutenir des décisions de santé plus intelligentes qui améliorent les résultats pour les patients. Les divers ensembles de données d’IQVIA offrent cette valeur dans un écosystème de données lié unique, répondant aux besoins uniques de RWD d’organisations comme la vôtre. Pour en savoir plus, visitez le site Web d’IQVIA et parlez à un expert dès aujourd’hui.
1. Deloitte. RWE se concentre sur la R&D, les premiers investissements commencent à porter leurs fruits. Consulté en mars 2021 sur https://www2.deloitte.com/us/en/insights/industry/health-care/real-world-evidence-study.html
2. Deloitte. RWE se concentre sur la R&D, les premiers investissements commencent à porter leurs fruits. Consulté en mars 2021 sur https://www2.deloitte.com/us/en/insights/industry/health-care/real-world-evidence-study.html
3. Deloitte: mission critique: les sociétés biopharmaceutiques accélèrent l’adoption, l’investissement et l’application de preuves dans le monde réel. Consulté en mars 2021 sur https://www2.deloitte.com/content/dam/insights/us/articles/4354_Real-World-Evidence/DI_Real-World-Evidence.pdf
4. MedTech Dive. La FDA vante l’utilisation de preuves du monde réel par Abbot, Medtronic dans l’analyse des décisions réglementaires. Consulté en mars 2021 sur https://www.medtechdive.com/news/fda-real-world-evidence-use-abbott-medtronic/596846/ 5. IQVIA. Sélection de données du monde réel. Consulté en mars 2021 sur https://www.iqvia.com/library/white-papers/selecting-real-world-data
6. IQVIA. Sélection de données du monde réel. Consulté en mars 2021 sur https://www.iqvia.com/library/white-papers/selecting-real-world-data
7. IQVIA. Recherche sur les données du monde réel et les sciences de la vie. Consulté en mars 2021 sur https://www.iqvia.com/locations/united-states/library/white-papers/real-world-data-and-life-sciences-research
8. IQVIA. Tirer parti des données du monde réel pour mesurer la gravité de la maladie. Consulté en mars 2021 sur https://www.iqvia.com/locations/united-states/blogs/2021/02/leveraging-real-world-data-to-measure-disease-severity