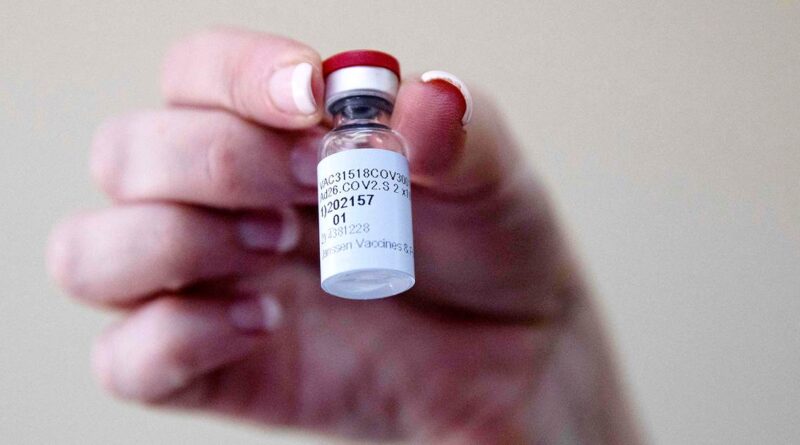
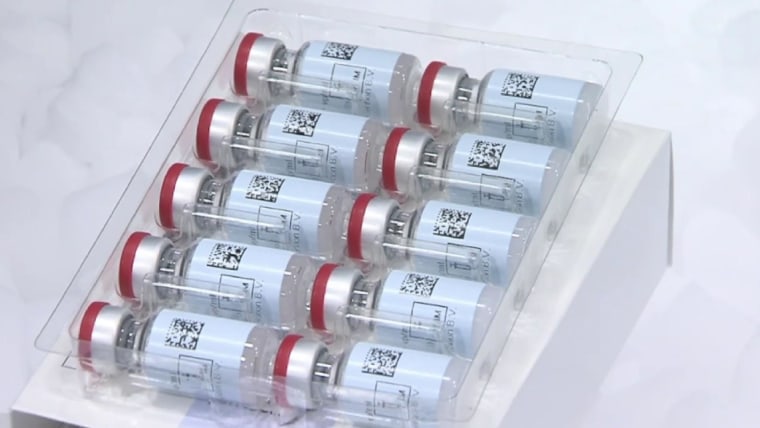
La FDA accorde une autorisation d’urgence au vaccin Johnson & Johnson
La Food and Drug Administration a accordé samedi une autorisation d’utilisation d’urgence au vaccin Covid-19 de Johnson & Johnson, l’ajout d’un troisième vaccin à l’arsenal américain pour lutter contre la pandémie.
«L’autorisation d’utilisation d’urgence d’aujourd’hui du vaccin Janssen Covid-19 est une autre étape importante alors que nous travaillons pour mettre fin à la pandémie de Covid-19», a déclaré le Dr Peter Marks, directeur du FDA Center for Biologics Evaluation and Research. «Guidés par notre examen attentif de la science et des données, nous avons déterminé que les avantages potentiels connus du vaccin l’emportent clairement sur ses risques potentiels connus.»
Couverture complète de l’épidémie de coronavirus
La décision intervient un jour après qu’un comité consultatif de la FDA a voté à l’unanimité en faveur de la recommandation du vaccin.
« Nous sommes dans une course entre la mutation du virus, avec la sortie de nouvelles variantes susceptibles de provoquer d’autres maladies, et son arrêt », a déclaré le Dr Jay Portnoy, professeur de pédiatrie à la faculté de médecine de l’Université du Missouri-Kansas City et un membre du comité consultatif.
« Moins il y a de personnes infectées par le virus, moins il a de chances d’émerger comme une souche plus virulente. »
Le président Joe Biden a publié une déclaration après l’annonce, qualifiant la décision de « nouvelle passionnante pour tous les Américains et de développement encourageant dans nos efforts pour mettre fin à la crise ».
Les doses devraient commencer à être expédiées lundi, à commencer par environ 4 millions d’entre elles. Johnson & Johnson, qui a développé le vaccin en partenariat avec Janssen Pharmaceuticals, a déclaré que 20 millions de doses seraient disponibles d’ici la fin du mois de mars.
Ce sera suffisant pour vacciner complètement 20 millions de personnes, car le vaccin Johnson & Johnson est administré en une seule dose. Les autres vaccins disponibles, de Pfizer-BioNTech et Moderna, sont administrés en deux doses chacun, à trois à quatre semaines d’intervalle.
Bien que le vaccin Johnson & Johnson soit administré en une seule dose, la société étudie l’impact d’une deuxième dose.
Vendredi, les membres du panel d’experts indépendants de la FDA se sont demandé ce qui se passerait si une formulation à deux doses était finalement autorisée.
Le Dr Paul Offit, expert en vaccins à l’hôpital pour enfants de Philadelphie, a suggéré qu’il pourrait être difficile de communiquer le changement à ceux qui n’ont reçu qu’une seule dose.
«Vous pouvez voir où cela pourrait dérouter les gens où ils pourraient penser: ‘Peut-être que je n’ai pas obtenu ce dont j’ai besoin?’»
Une analyse de la FDA, publiée en ligne mercredi, a révélé que le vaccin était sûr et efficace. Le seul coup s’est avéré efficace à 86% pour prévenir les maladies graves. Aux États-Unis, le vaccin s’est avéré efficace à 72% pour prévenir les maladies modérées à sévères. En Afrique du Sud, où une variante inquiétante circule, ce nombre était plus bas: 64 pour cent.
«Les gens devraient prendre le vaccin auquel ils ont accès», a déclaré Janet Woodcock, commissaire par intérim de la FDA. « Tous ces vaccins répondent à nos normes d’efficacité. »
Téléchargez l’application NBC News pour une couverture complète de l’épidémie de coronavirus
Le Dr Richard Besser, président et chef de la direction de la Fondation Robert Wood Johnson et ancien directeur par intérim des Centers for Disease Control and Prevention, a applaudi la décision de la FDA.
« Avec trois vaccins Covid-19 désormais disponibles, le nombre de cas et de décès dans le pays continuant de baisser et le Congrès prenant des mesures pour approuver une aide économique supplémentaire, absolument nécessaire, je n’ai jamais été aussi encouragé à l’idée que nous pourrions enfin franchir le cap. cette pandémie », a-t-il déclaré dans un communiqué.
Pourtant, Besser a déclaré que les Américains doivent rester vigilants, adhérer au port de masque, distancer et limiter les déplacements. «La fin de la pandémie et le moment où elle se terminera, comme elle l’a toujours été, dépend en grande partie de nous.
En décembre, la FDA a autorisé les vaccins Covid-19 de Pfizer-BioNTech et Moderna. Deux autres vaccins, d’AstraZeneca et de Novavax, achèvent des essais cliniques de phase 3 et devraient demander l’autorisation de la FDA au printemps.
Suivez NBC HEALTH sur Twitter & Facebook.